祝贺苏丽云和许静怡的文章在Cell Death Discovery发表2024-04-22 11:20:44
线粒体通透性转换(mitochondrial permeability transition, mPT)介导的线粒体功能障碍在各种人类疾病中起着关键作用。然而,由于Bax/Bak诱导的线粒体外膜通透化(mitochondrial outer membrane permeabilization, MOMP)所造成的干扰,以及目前对线粒体通透性转换孔(mitochondrial permeability transition pore,mPTP)结构及其各组成成分复杂相互作用的知之甚少,使得mPT发生机制的复杂细节和事件顺序未得到解析。近日,我们课题组利用自行研发的纳米流式细胞术(nano-flow cytometry, nFCM),通过单线粒体水平的多参数同时分析,揭示了线粒体mPT发生过程中mPTP的开启、线粒体膜电位(ΔΨm)的下降、细胞色素c(Cyt c)的释放等重要事件的时间顺序,发现了mPT多途径同时诱导细胞凋亡的现象,有望成为一种创新的癌症治疗和干预策略,研究成果以“Nano-flow cytometry unveils mitochondrial permeability transition process and multi-pathway cell death induction for cancer therapy”为题,在Cell Death Discovery期刊上发表(Cell Death Discovery (2024) 10:176 )。
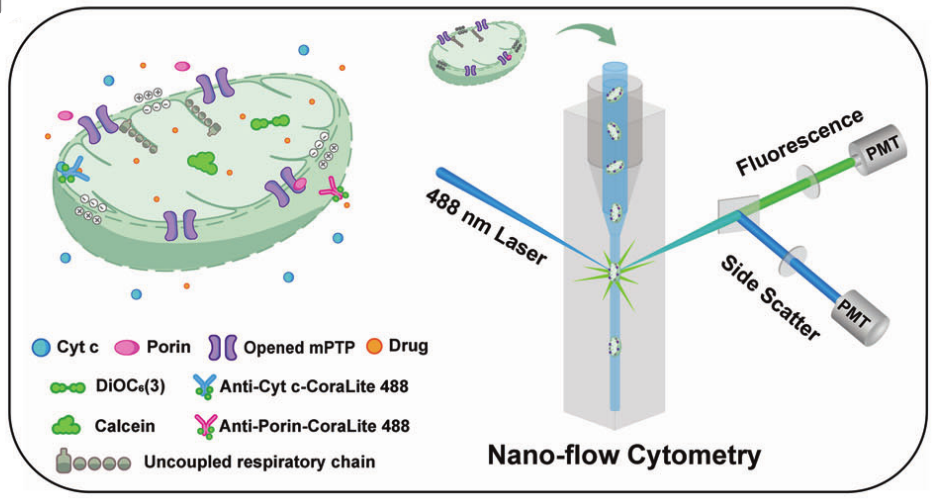
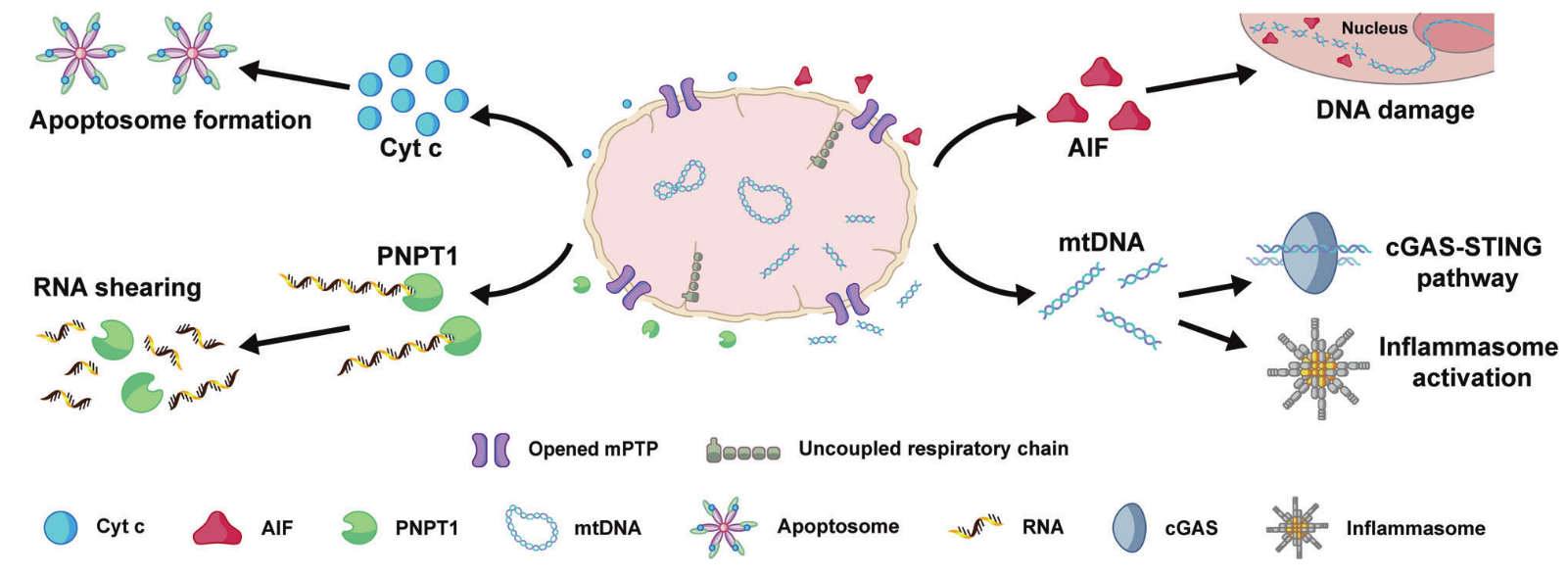
首先,作者从HeLa细胞中分离线粒体,并验证了其氧化磷酸化功能正常。采用Ca2+刺激提纯的HeLa细胞线粒体,分别使用荧光染料或荧光抗体标记,利用nFCM对mPTP 开放、ΔΨm下降、Cyt c释放和孔蛋白(porin)减少的情况进行单线粒体水平的检测,构建mPT诱导线粒体功能障碍的检测方法。结果表明,桦木酸(BetA)和抗霉素A可以通过mPT介导的机制直接诱导线粒体功能障碍,而顺铂和紫杉醇则不能。nFCM分析还揭示了BetA主要通过降低Bcl-2和Bcl-xL蛋白水平以及提高ROS含量诱导mPTP开启、ΔΨm下降和Cyt c释放。接下来,利用BetA的剂量和时间依赖性策略,探究了mPT介导的线粒体功能障碍的详细过程及其机制,发现ΔΨm降低是Cyt c释放的上游事件。在细胞水平使用shRNA技术敲低Bax和Bak蛋白表达的实验进一步验证了ΔΨm降低、Cyt c释放这两个事件的时间先后顺序。最后,通过nFCM测定发现mPT诱导的线粒体功能障碍能通过释放凋亡诱导因子(apoptosis inducing factor, AIF)、多核糖核苷酸核苷转移酶1(polyribonucleotide nucleotidyltransferase 1, PNPT1)和mtDNA等多种途径诱导细胞死亡。此外,有趣的是,即使在敲出Bax/Bak的情况下,BetA也能诱导caspase-independent细胞死亡,从而克服药物耐药。这进一步验证了靶向mPT诱导的线粒体功能障碍在克服癌细胞耐药性和\广谱癌症治疗中的潜力。
厦门大学化学化工学院苏丽云博士和许静怡博士为论文的共同第一作者。该工作得到国家自然科学基金委项目(21934004和21627811)和科技部重点研发计划专项(2021YFA0909400)的资助。论文链接:https://www.nature.com/articles/s41420-024-01947-y